史上首款免费临研一体 化解决方案(EDC+CTMS)
史上首款免费临研一体化解决方案(EDC+CTMS)
H5,H5页面制作工具

- 史上首款免费临研一体化解决方案(EDC+CTMS)
- 400-1580-300 BD@totrial.com
- 2018

- Totrial临床试验数据采集系统满足FDA 21CFR规则以及CNDA相关指导原则和法规;
- 21CFR验证
- TT临床试验数据采集系统提供API接口,能够实现客户的对接需求;
- 系统对接
- 无需IT基础;短期培训即可掌握建库和数据核查的基本要求;大幅降低研究成本;
- 敏捷核查建库

- 系 统 简 介
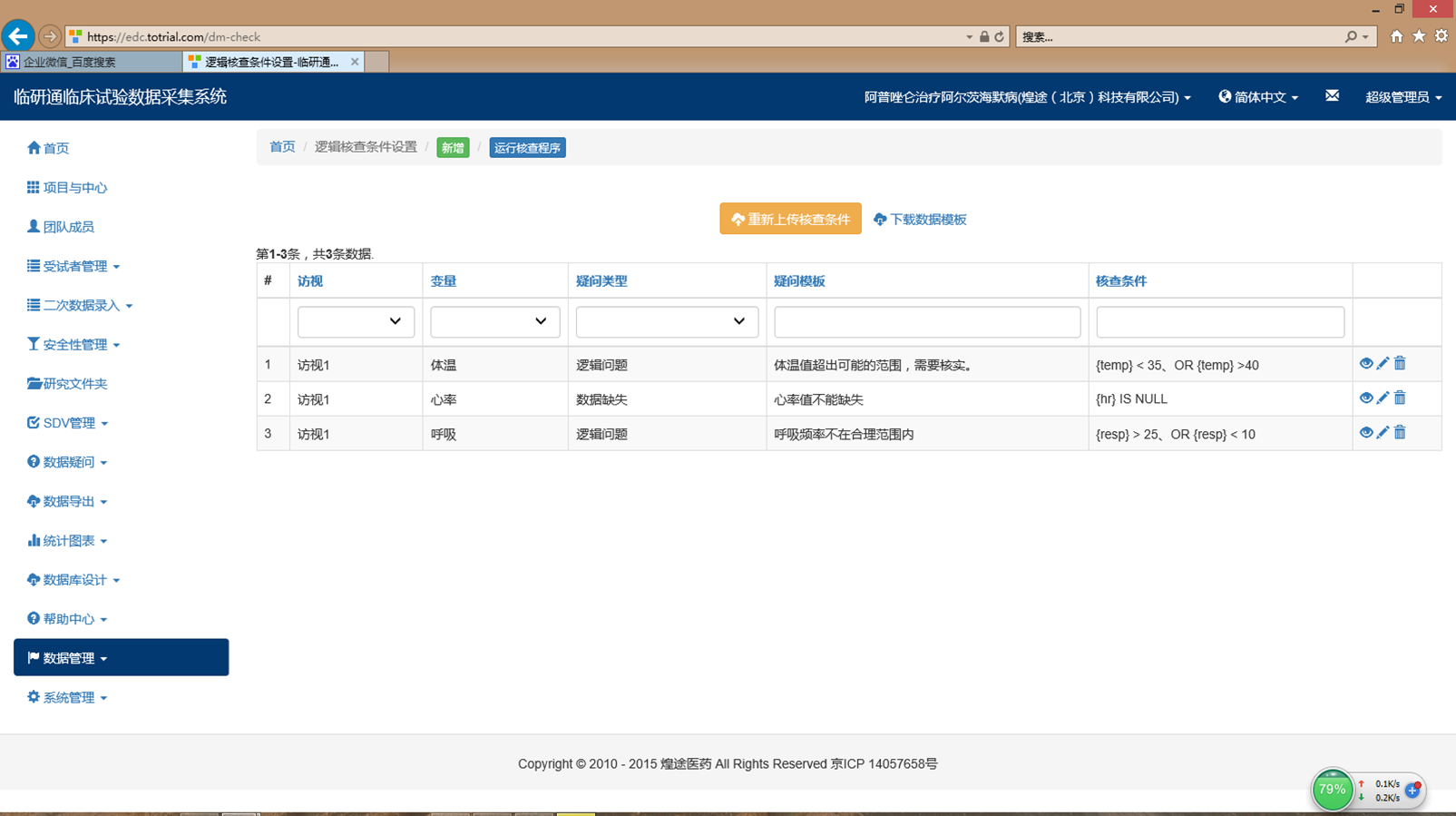
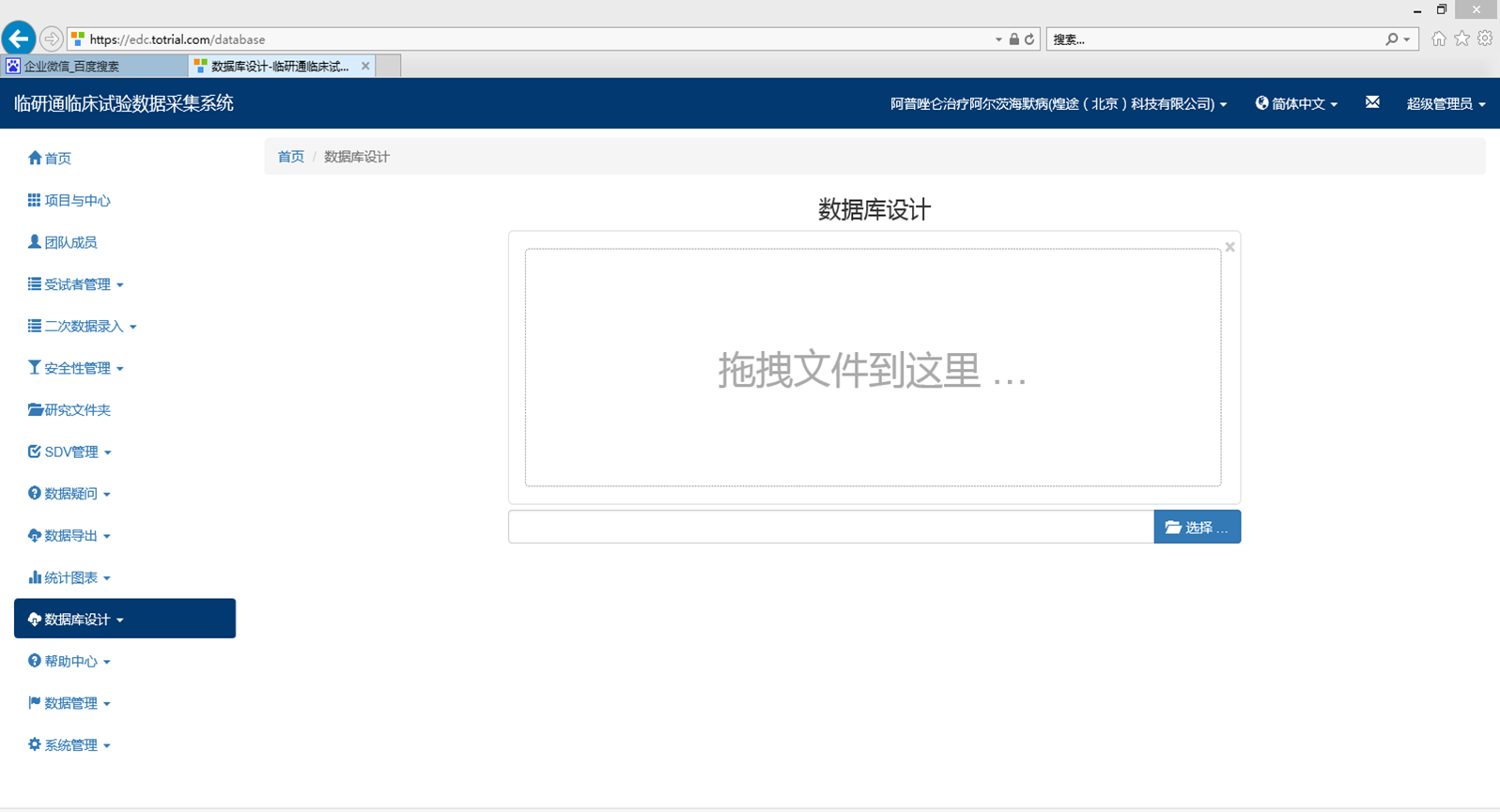
- 数 据 库 设 计
- 程序BUG反馈单价:免费
- 数据导出单价:1000元/次
- 基础培训单价:免费包括视频、文字等满足软件使用的基本培训以及随软件版本更新的培训服务
- 其他周期性费用单价:RMB2000/年/项目包括软件维护、数据备份、数据容灾恢复、服务器使用费用等
- 基础软件使用单价:免费包括EDC系统的全部常用功能

- 基 础 服 务
- SOP文件授权RMB20000/项目。
- 6
- 数据管理计划单价:RMB20000/项目包含数据管理计划以及修改记录等。
- 5
- 4
- 3
- 2
- 1
- CRF注释单价:RMB20000/项目完整的CRF注释。
- 高频备份与导出价格:需面议基础的每日数据备份可以满足绝大多数要求,如需更高频度的数据备份,需另付费用。
- 数据接口API单价:RMB500/项可集成在其他软件中,提供详细文档。仅收取API配置、认证的手续费。基础的数据调用频度和调用IP受限,可满足绝大多数使用,若需要进一步开放限制需另议。
- 一对一培训单价:RMB5000/次包含基础培训以及一些软件疑难问题解答,工时约在6小时左右。若为现场培训,本报价不含差旅费。
- 增 值 服 务
- 过程控制文件RMB50000/项目
- 6
- 人工质疑及数据管理报告价格:需面议根据实际项目情况进行。
- 5
- 4
- 3
- 2
- 1
- 数据核查程序撰写单价:RMB200元/数据项,含数据核查程序撰写、测试数据准备、测试报告准备。
- 数据核查计划撰写价格:RMB30000-50000/项目,根据定稿的研究方案和CRF撰写数据核查计划。
- 数据库建库(含测试)单价:RMB30000/项目包括模拟数据、数据库建库、数据库测试、测试脚本执行、测试报告准备。前提是需要客户提供好完整的CRF注释文档.
- 数据库建库(不含测试)单价:RMB10000/项目仅包含建库, 前提是需要客户提供好完整的CRF注释文档。
- 增 值 服 务
- 基本操作
- 数据录入
- 疑问管理
- 查询与导出
- 基本操作
- 目 录contents
- 账号获取与登录界面功能区介绍密码修改与重置
- 01
- 基 本 操 作
- 登录网址:http://edc.totrial.com
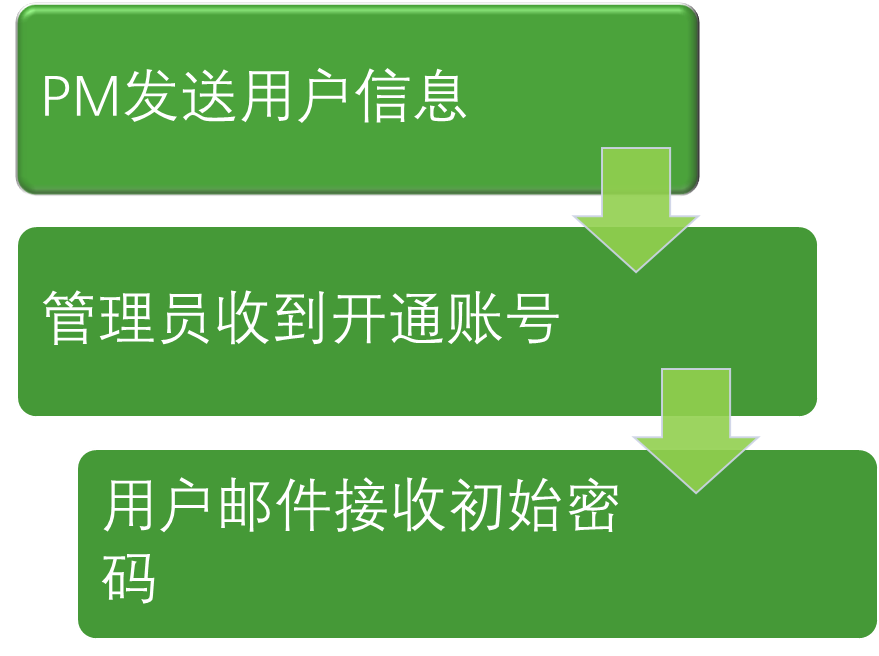
- 本系统不开放对外注册功能,在研究开始时,PM将项目相关人员的姓名,项目角色,研究中心和邮箱信息发送给系统管理员,系统管理员收到后开通账号。在项目开展期间,项目人员变动,PM应及时邮件通知管理员更改相应权限。
- 1.1
- 账 号 注 册 与 登 录

- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
- 1.1
- 账 号 注 册 与 登 录
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
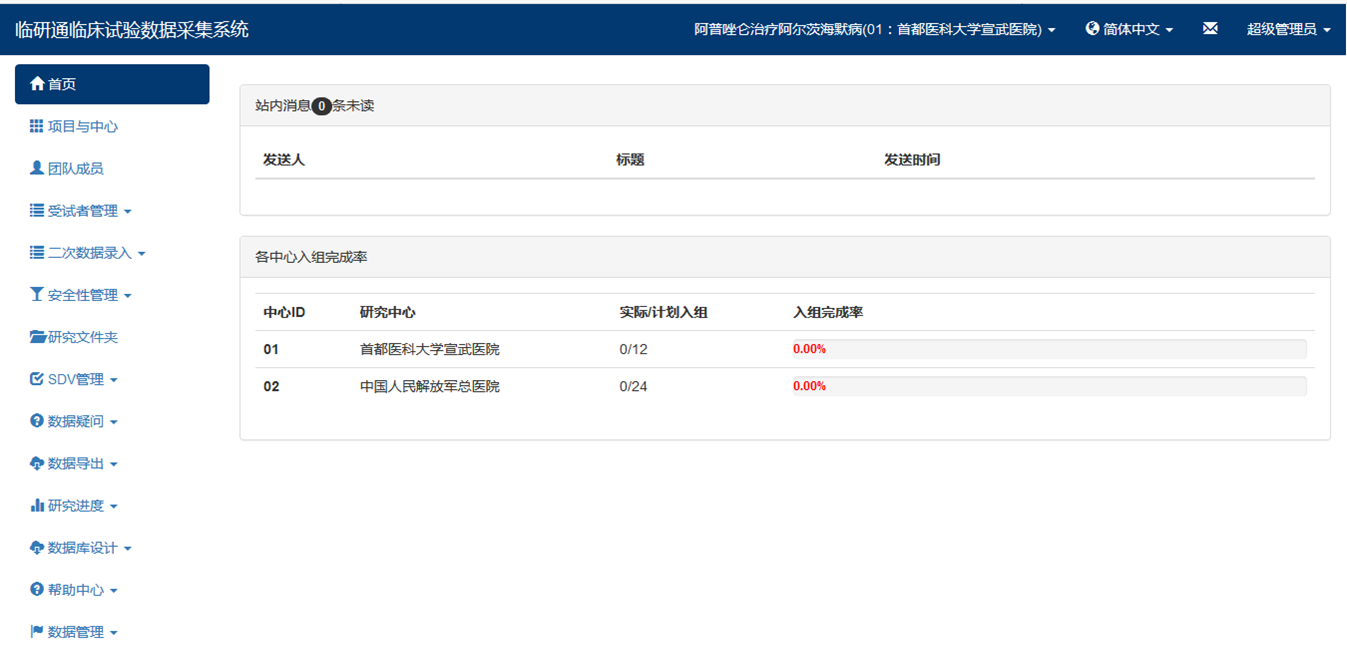
- 1.2
- 界 面 功 能 区 介 绍

- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
- 1.2
- 界 面 功 能 区 介 绍
- 重置密码
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
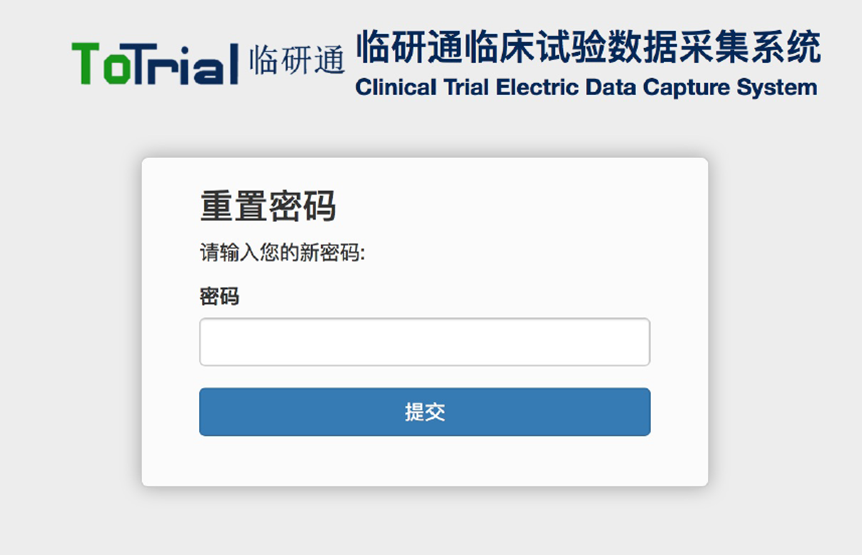
- 1.3
- 密 码 修 改 与 重 置
- 02
- 受试者CRF录入SAE录入错误修改
- 数 据 录 入
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
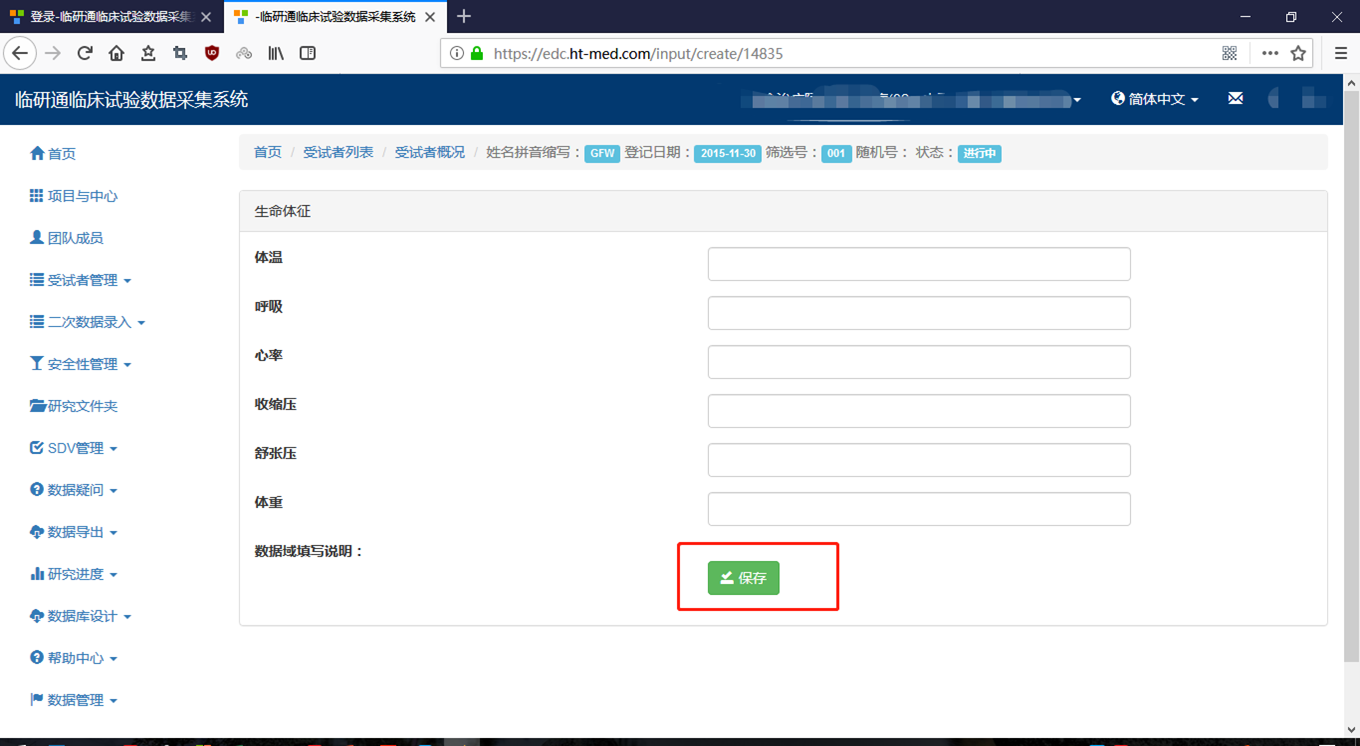
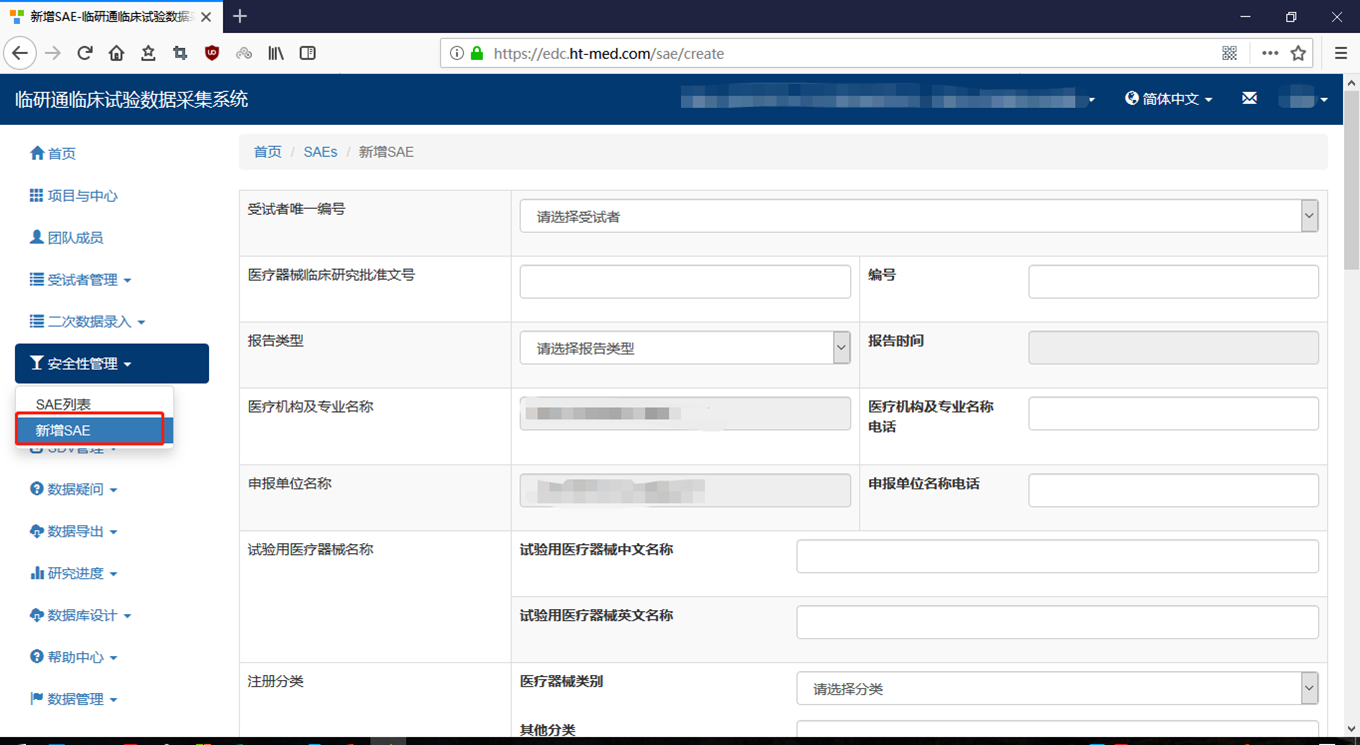
- 2.1
- 受 试 者 CRF 录 入
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
- 2.2
- 受 试 者 CRF 录 入

- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
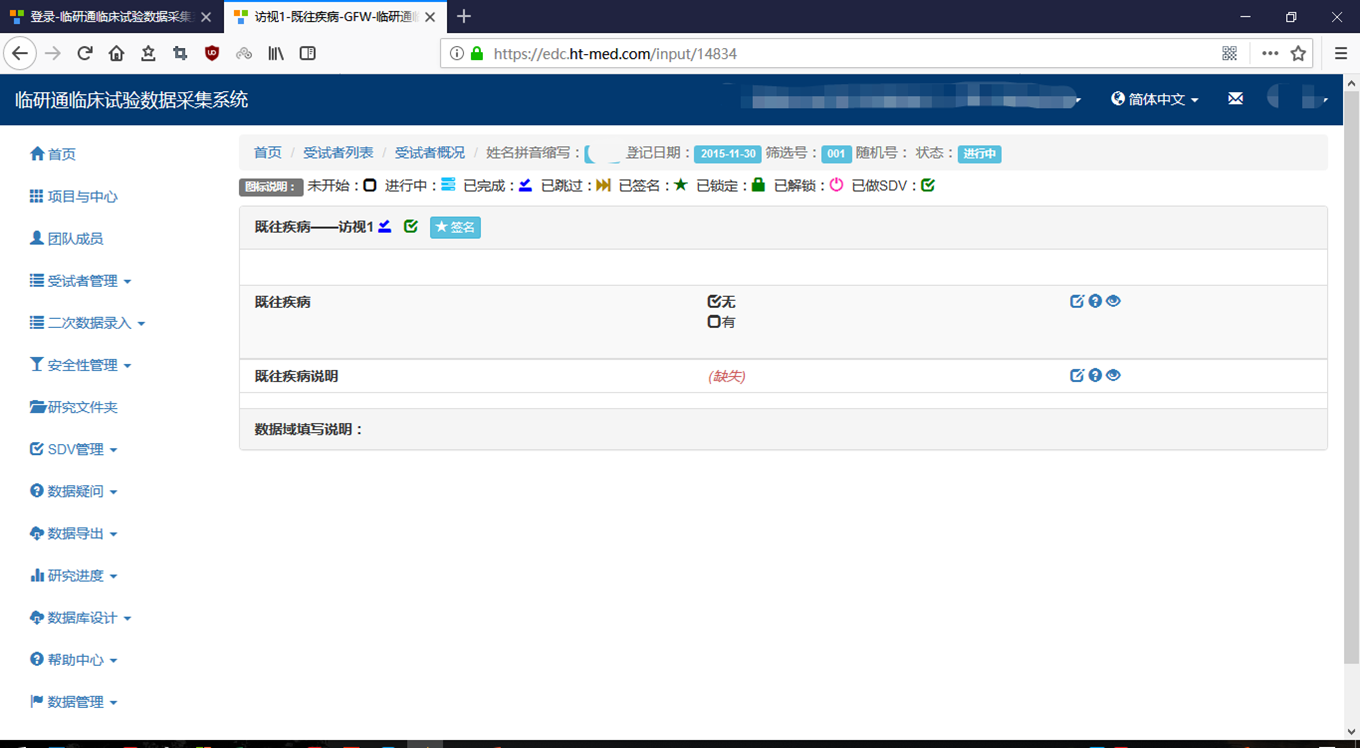
- 2.3
- 数 据 改 错
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
- 2.4
- 数 据 改 错
- 03
- 疑问管理疑问统计
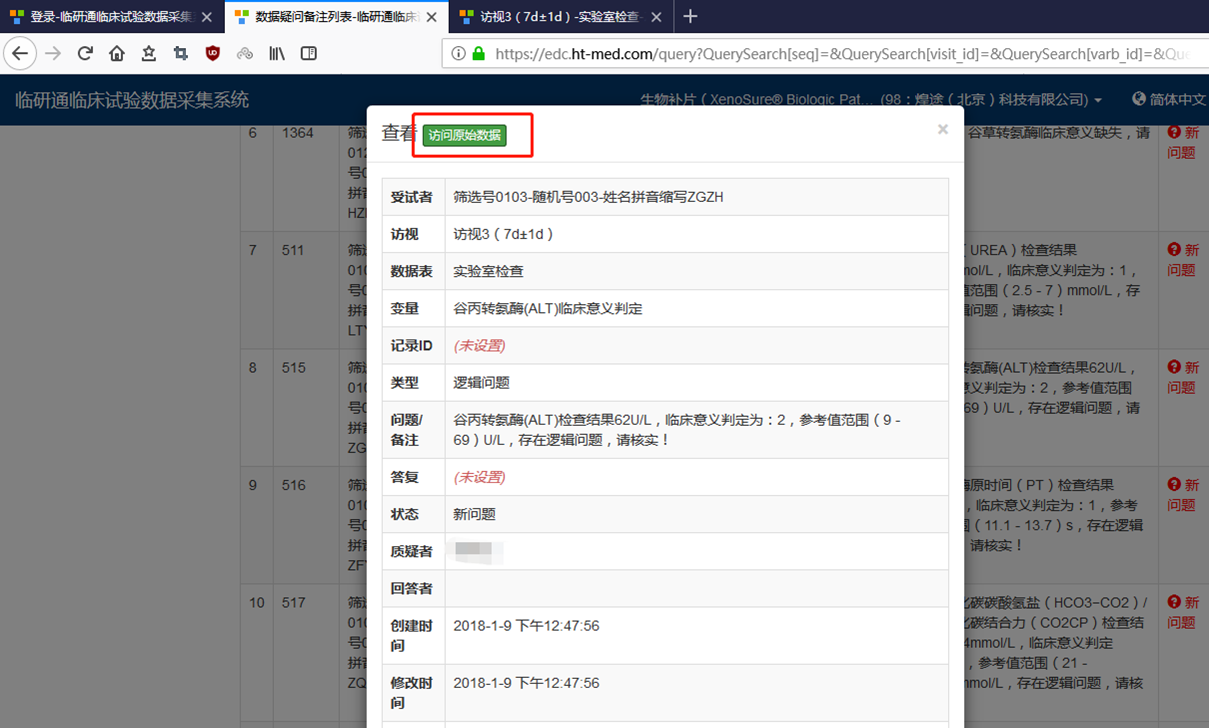
- 疑 问 管 理
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
- 3.1
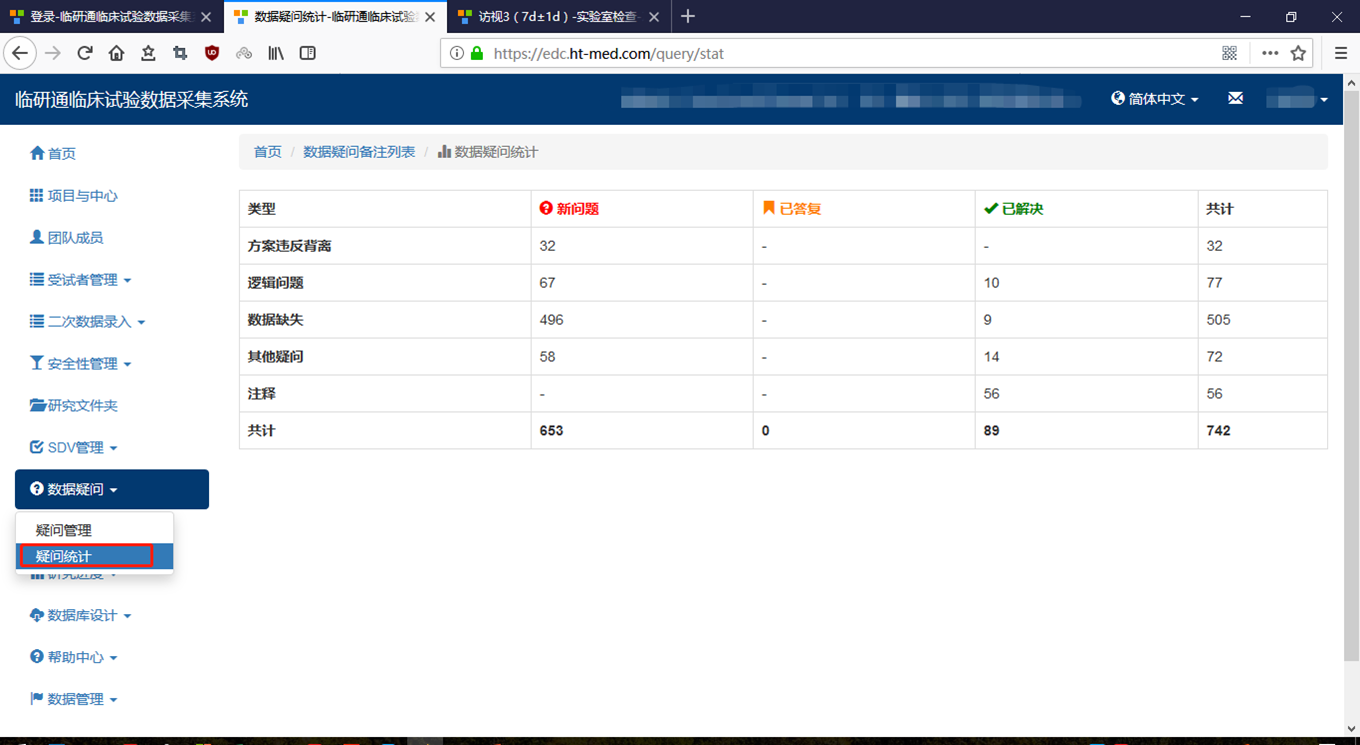
- 疑 问 统 计
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
- 3.2
- 疑 问 统 计
- 04
- 数据导出统计图表
- 查 询 与 导 出
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
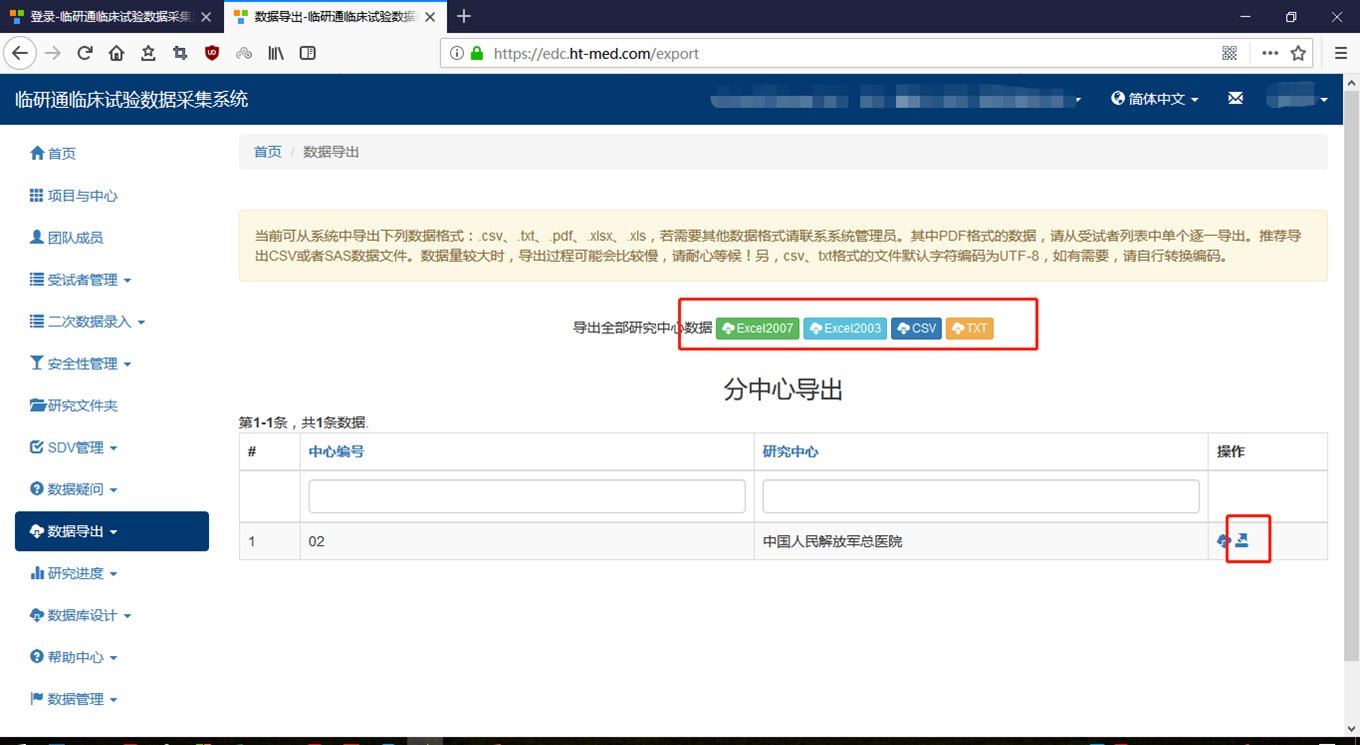
- 4.1
- 数 据 导 出
- 登录网址:http://edc.totrial.com
- 临研通临床试验数据采集系统Clinical Trial Electric Data Capture System
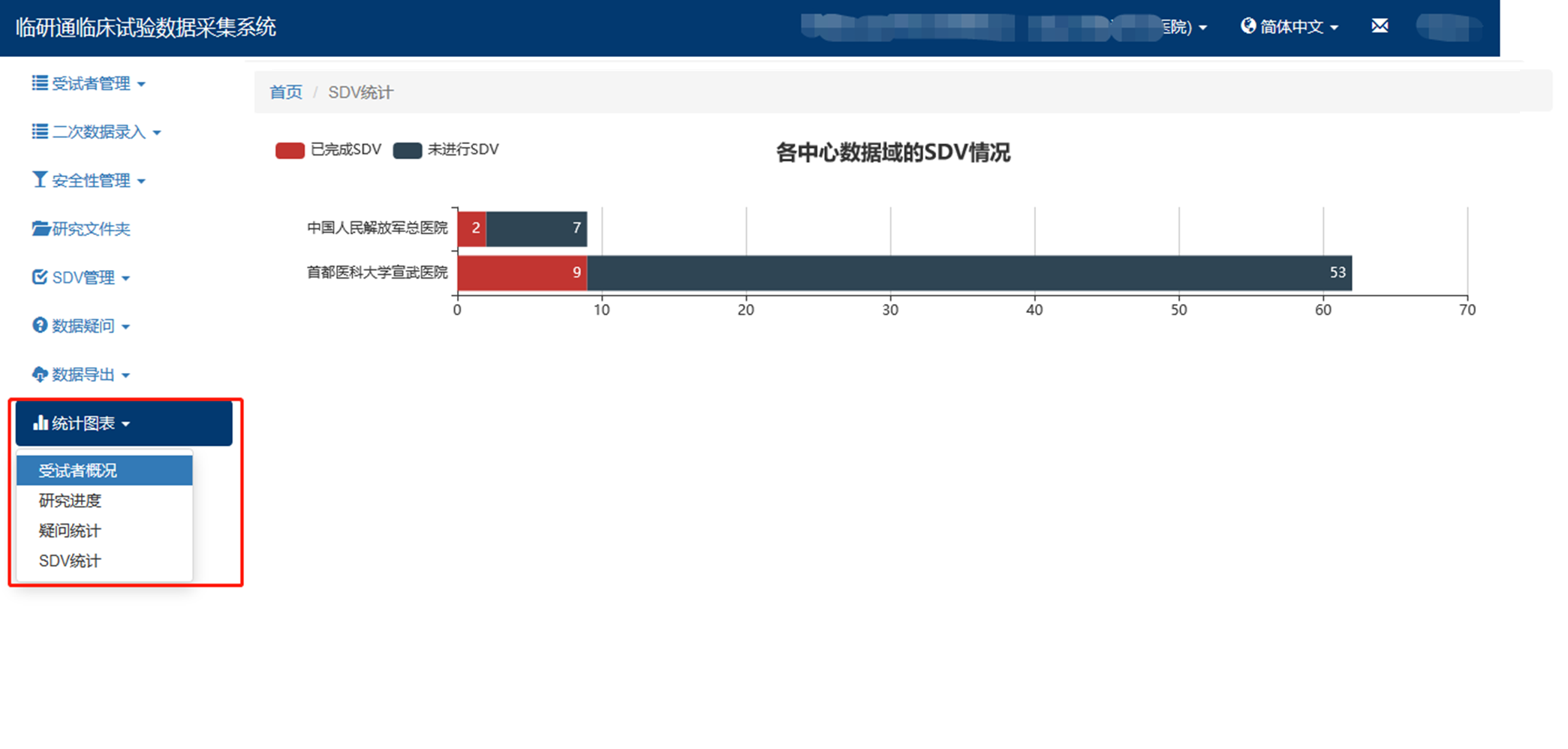
- 4.2
- 统 计 图 表
- 煌途医药集团旗下400-1580-300www.HT-Med.com
- 400-1580-300 BD@totrial.com

谢 谢 观 看 !